
Проблема нейропатической боли приобретает все большую актуальность для клиницистов разного профиля, что связано с широким распространением патологии и трудностями в достижении стойкого терапевтического эффекта. Несмотря на большое количество фармакологических препаратов, рекомендованных для лечения пациентов с нейропатической болью, выбор оптимальной схемы лечения часто вызывает затруднения у клиницистов.
А.Г. Хиц
Редакция журнала «Украинский медицинский журнал»
Проблема нейропатической боли приобретает все большую актуальность для клиницистов разного профиля, что связано с широким распространением патологии и трудностями в достижении стойкого терапевтического эффекта. Несмотря на большое количество фармакологических препаратов, рекомендованных для лечения пациентов с нейропатической болью, выбор оптимальной схемы лечения часто вызывает затруднения у клиницистов. В статье представлены современные подходы к терапии нейропатической боли, описана эффективность и безопасность применения современных габапентиноидов на примере прегабалина (Неогабин) и нуклеотидов в сочетании с витамином B12 и фолиевой кислотой (Нейристон®).
Хронический болевой синдром – чрезвычайно распространенное состояние в популяции, снижающее качество жизни пациентов, ограничивающее работоспособность и связанное со значительными прямыми и косвенными экономическими затратами. Несмотря на пристальный интерес к этой проблеме и достигнутый успех в менеджменте пациентов этой категории, патогенетическая многогранность хронического болевого синдрома часто представляет проблему на пути формирования адекватной терапевтической тактики.
По патофизиологическим механизмам развития различают ноцицептивную и нейропатическую боль (НБ). Ноцицептивный компонент боли формируется в результате раздражения периферических болевых рецепторов. Триггерами могут выступать внешние (термические, механические, химические) и внутренние (медиаторы воспаления, локальный ацидоз при мышечном спазме) факторы. Нейропатический компонент болевого синдрома возникает при поражении или нарушении функции периферических или центральных нервных структур, участвующих в контроле и проведении болевой импульсации. НБ обычно является хронической и развивается за счет периферической и центральной сенситизации ноцицептивных нейронов. Механизмы развития НБ делят на центральные и периферические, в зависимости от локализации пораженной нервной структуры, при этом клинической основой может выступать широкий спектр заболеваний и патологических состояний (таблица).
|
НБ |
|
|---|---|
|
Периферическая |
Центральная |
|
|
Проблема НБ приобретает все большую актуальность для клиницистов, что напрямую связано с распространением этой патологии и трудностями в достижении устойчивого терапевтического эффекта. Так, по имеющимся данным, распространенность НБ в общей популяции составляет 7–8%, а на неврологическом приеме пациенты с НБ составляют около 18%. НБ выявляют у 30-40% пациентов онкологического профиля, у каждого 4-го пациента с сахарным диабетом (СД), у каждого 10-го пациента, перенесшего инсульт, и у значительной доли лиц с хронической болью в нижней области спины – 10-37%.
Среди широкого спектра факторов, дающих толчок формированию хронической НБ, особое место принадлежит боли в нижнем участке спины. Чаще (у 51–80% пациентов) боль в спине имеет локализацию в пояснично-крестцовом отделе. При этом, в большинстве случаев, НБ неспецифическая и полиэтиологическая по своей природе. В патогенезе её формирования нейропатический компонент занимает около 60%. Это объясняет феномен разного ощущения боли у пациента: от умеренного до выраженного и изнурительного, в зависимости от преобладания одного из механизмов формирования болевого синдрома.
Нейропатический компонент болевого синдрома связан с повреждением нервных структур корешка, компрессией костными структурами позвоночника, интерневральным отеком, ишемией или воспалением. При этом происходит повреждение как миелиновой оболочки нервного волокна, так и его самого. Повреждение всех сенсорных периферических волокон (волокон Aβ, Aδ и C) с нарушением трансдукции и передачей импульсации из-за нарушения функции ионных каналов приводит к формированию очагов патологического возбуждения. На рис. 1 отображена блок-схема НБ.
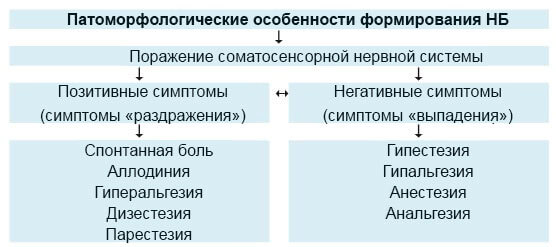
Другим фактором, приводящим к возникновению НБ, является ДПНП, которая является частым осложнением СД. По данным большого популяционного опроса, ДПНП регистрируют у 30% пациентов с СД 1-го и у 36–40% — 2-го типа. При впервые выявленном СД 2 типа ДПНП диагностируют у 14–20% больных, при длительности СД > 15 лет количество пациентов с ДПНП достигает 50–70%.
ДПНП может быть острой и хронической, симметричной и асимметричной, асимптомной или болевой. Хроническая дистальная симметричная сенсорная и сенсомоторная полинейропатия – наиболее частые ее варианты. Именно эти две формы чаще всего сопровождаются болевым синдромом, отмечаемым в 20–50% случаев. Боль при ДПНП вызывает нарушение сна, развитие депрессии, эректильную дисфункцию у мужчин, снижение физической и социальной активности, значительное ухудшение качества жизни пациентов. С увеличением интенсивности боли, ухудшаются показатели физического и когнитивного здоровья, что приводит к значительному снижению повседневной активности, работоспособности и раннему выходу на пенсию. Несмотря на то, что нормогликемия считается главным условием предотвращения развития ДПНП, эта задача не всегда выполнима, и заболевание обычно прогрессирует.
Проблема НБ состоит в том, что этот тип болевого синдрома крайне тяжело поддается терапии и не всегда удается полностью устранить болевой синдром. Нередко у этих пациентов нарушается сон, развивается депрессия и тревога, снижается качество жизни и трудоспособность. Многие из них долгое время терпят боль до того, как начинают получать адекватную терапию.
Лечение пациентов с НБ при множественных сопутствующих заболеваниях — сложный мультидисциплинарный процесс, требующий медикаментозной терапии, психологической реабилитации и физиотерапевтического воздействия. Несмотря на доказанную низкую эффективность нестероидных противовоспалительных препаратов (НПВП) и анальгетиков у этих больных, около ⅔ из них получают указанные препараты. Неправильный выбор тактики лечения у больных НБ приводит к снижению его эффективности и существенному увеличению продолжительности лечения и расходов (Tolle T. et al., 2006). При этом лишь незначительная часть врачей используют в своей клинической практике полный перечень рекомендованных лекарственных средств, которые можно было бы применить в качестве препаратов первой линии для купирования НБ (Martinez V. et al., 2014).
Согласно современным рекомендациям, габапентиноиды (габапентин и прегабалин), трициклические антидепрессанты и ингибиторы обратного захвата серотонина и норадреналина являются препаратами первой линии в терапии в случае НБ. Препараты второй линии – трамадол и опиоиды, ведь при их применении имеется повышенный риск развития неблагоприятных побочных эффектов, медицинских осложнений и зависимости. Каннабиноиды рекомендованы как терапия третьей линии, поскольку на сегодня недостаточно качественных данных по эффективности и безопасности их применения в терапии в случае НБ. К препаратам четвертой линии относят метадон, противосудорожные препараты с более низкими показателями эффективности (ламотриджин, лакосамид), тапентадол и ботулинический токсин.
Согласно рекомендациям Европейской федерации неврологических обществ (European Federation of Neurological Societies), препаратами выбора при лечении пациентов с НБ являются антиконвульсанты и антидепрессанты. Эти препараты обеспечивают патогенетическую терапию при НБ, устраняя чрезмерную возбудимость структур периферической и центральной нервной системы. На основании систематического обзора и метаанализа всех исследований, проведенных с 1966 г., включая неопубликованные работы, прегабалин, габапентин, дулоксетин и различные трициклические антидепрессанты имеют прочную основу для применения и рекомендованы в качестве препаратов первой линии при терапии НБ (Finnerup N.B., Attal N., 2016).
Об эффективности применения антиконвульсантов I поколения для симптоматического лечения при НБ известно много лет. Их эффект обусловлен блокировкой натриевых каналов и подавлением эктопической активности в пресинаптических сенсорных нейронах. Исследования карбамазепина, фенитоина, вальпроата показали их эффективность при болевой форме ДПНП, однако такие нежелательные побочные явления, как головокружение, двоение в глазах, диарея, когнитивные расстройства не позволяют рассматривать их как терапию первой линии. В последние годы доказана высокая эффективность применения антиконвульсантов II поколения, в частности прегабалина, в терапии при НБ. Так, результаты многих систематических осмотров свидетельствуют, что среди лекарственных средств, применяющихся в лечении пациентов с НБ, наиболее эффективны с точки зрения клинициста и безопасности для пациента препараты группы габапентиноидов, в частности прегабалин и габапентин, что делает их препаратами выбора в терапии пациентов с НБ (Finnerup N.B. et al., 2005). Полученные данные об их высокой эффективности и безопасности, подтвержденные во многих исследованиях, стали поводом для создания европейских протоколов по лечению в случае боли в нижнем участке спины с нейропатическим компонентом (Finnerup N.B. et al., 2005; Attal N. et al., 2010; Martinez V. et al., 2010). Французское общество по борьбе с болезнями (Société Française d'Etude et de Traitement de la Douleur) создало рекомендации по менеджменту пациентов с НБ, ориентированные на врачей общей практики, с целью повышения эффективности лечения пациентов с НБ на всех уровнях, включая амбулаторную помощь (Martinez V. et al., 2010), в которых прегабалин указан как препарат первой линии. Сегодня Европейская комиссия и Управление по контролю за пищевыми продуктами и лекарственными средствами США (Food and Drug Administration — FDA) одобрили прегабалин как основное средство для лечения в случае периферического НБ (Moulin D.E. et al., 2007).
Препарат позволяет достаточно быстро и эффективно купировать такие проявления НБ при ДПНП как тревога, депрессия, нарушение сна, улучшить общее состояние и качество жизни пациентов, что доказано в ряде клинических исследований. Так, в рандомизированном контролируемом клиническом исследовании J. Rosenstock и соавторы (2004) оценивали эффективность прегабалина по сравнению с плацебо у 146 пациентов с ДПНП. В течение 8 недель пациенты основной группы (n=76) получали прегабалин в дозе 300 мг/сут, а группы контроля (n=70) — плацебо. Результаты продемонстрировали достоверное уменьшение выраженности болевого синдрома и улучшение показателей качества жизни (улучшение общего состояния, восстановление сна, снижение тревоги) у пациентов, принимавших прегабалин, а также его хорошую переносимость.
Данные по эффективности, безопасности и переносимости прегабалина в разном диапазоне доз при болевой форме ДПНП продемонстрированы в объединенном анализе семи двойных слепых рандомизированных плацебо-контролируемых исследований с участием 9 тыс. больных. Доза прегабалина составляла 150, 300 или 600 мг/сут, разделена на 2 или 3 приема, продолжительность лечения – 5-13 нед. Во всех исследованиях прегабалин показал высокую эффективность, по сравнению с плацебо, не только значительно уменьшая интенсивность болевого синдрома, но и восстанавливая нарушенный сон (Freeman R. et al., 2008).
Кроме того, во многих исследованиях показана не только высокая эффективность прегабалина в лечении при наличии НБ у пациентов с заболеваниями спины, но также высокая безопасность, по сравнению с другими препаратами. Так, в исследовании, проведенном в Японии в 2016 г., оценивали анальгезирующий эффект прегабалина, в зависимости от назначенной дозы. Первоначальной конечной точкой исследования был прямой анальгезивный эффект – уменьшение выраженности болевого синдрома в ногах при оценке с использованием визуальной аналоговой шкалы (Visual analogue scale – VAS) (Orita S. et al., 2016). Результаты продемонстрировали, что к 6-й неделе лечения у 82,4% пациентов выраженность боли значительно уменьшилась и в среднем по шкале VAS находилась в пределах ≤ 30: VAS 0 мм достигнут у 17,5%, высокий уровень ремиссии (10–20 мм) – у 38,6%, умеренный (30-40 мм) – у 26,3% пациентов. Отмечены также изменения других физических параметров пациентов. Значительно увеличилась дистанция ходьбы, хотя этот показатель не имел статистической достоверности.
В другом рандомизированном плацебо-контролируемом исследовании, проведенном R. Baron и соавторами (2010), оценивали клиническую эффективность и безопасность применения прегабалина по сравнению с плацебо в лечении 364 пациентов с пояснично-крестцовой радикулопатией, из них 79,7% — с протрузией межпозвоночного диска. В ходе исследования 36,8% пациентов получали НПВП, 13,4% – опиоиды, 21,4% – парацетамол. Прегабалин назначали в дозе 150–600 мг/сут 182 пациентам, остальные 182 получали плацебо. Длительность исследования составляла 77 дней. Динамику состояния оценивали по степени выраженности болевого синдрома на 28 день лечения и в конце исследования на основании выраженности диссомнических и тревожно-депрессивных расстройств, ассоциированных с болевым синдромом. Исследование продемонстрировало несомненное преимущество в группе пациентов, получавших прегабалин. Уже на 28-й день лечения пациенты отметили существенное уменьшение выраженности боли, а на 77-й день – достоверное уменьшение выраженности расстройств, ассоциированных с болевым синдромом: нарушений сна, тревоги и депрессивных расстройств (рис. 2–3). Кроме того, прегабалин продемонстрировал не только высокую анальгезивную активность, но и эффективность в отношении сопутствующих аффективных расстройств и инсомнии у пациентов с болевым синдромом при радикулопатии.
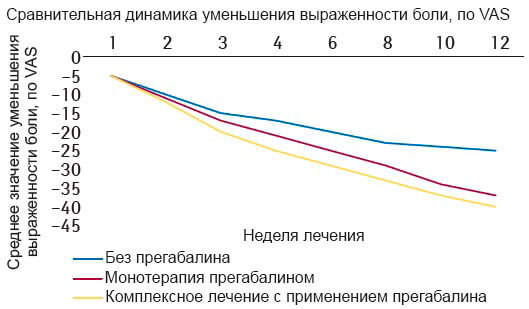
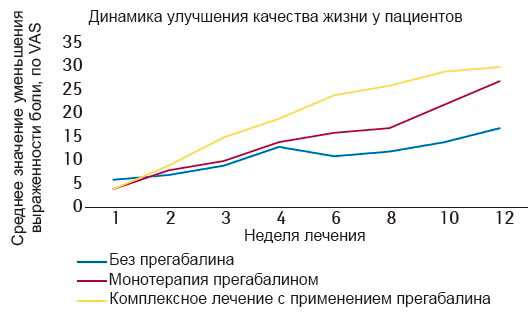
Одним из представителей прегабалина на рынке Украины является Неогабин производства фармацевтической компании «ACINO» — современный антиконвульсант, особенностями которого является оптимальный профиль безопасности и эффективности, быстрое начало действия, эффективность стартовой дозы и дозозависимый эффект. Неогабин производится на отечественном заводе компании на инновационном оборудовании в соответствии со стандартами GMP. Препарат зарекомендовал себя как эффективное средство для лечения НБ у взрослых пациентов при повреждении периферической и центральной нервной системы, эпилепсии (как дополнительная терапия парциальных судорожных приступов с вторичной генерализацией или без таковой), генерализованном тревожном расстройстве и фибромиалгии. Прегабалин является аналогом γ-аминомасляной кислоты, который связывается со вспомогательной субъединицей (α2-δ-белок) потенциалзависимых кальциевых каналов в центральной нервной системе, активно замещая [3H]-габапентин. Прегабалин тормозит высвобождение возбуждающих нейромедиаторов и тем самым блокирует передачу болевых импульсов на уровне задних рогов и на более высоких уровнях центральной нервной системы. Способность проявлять эффекты только в определенных участках нервной системы (коре головного мозга, обонятельных луковицах, гипоталамусе, гиппокампе, мозжечке, задних рогах спинного мозга) определяет его эффективность в подавлении болевых ощущений, а также развитии многих психосоматических расстройств (Attal N. et al., 2006).
Регенерация и восстановление миелиновой оболочки после повреждения является важным элементом лечения пациентов с периферической нейропатией, которая характеризуется потерей моторной и сенсорной функции дистальных отделов периферических нервов. Поэтому патогенетически обосновано применение субстанций, обладающих репаративной/протекторной активностью в отношении нервного волокна. Важную роль в клеточном метаболизме нервного волокна играют пиримидиновые нуклеотиды, в частности уридин и цитидин — низкомолекулярные структурные элементы, которые играют фундаментальную роль в процессах метаболизма.
Механизм действия нуклеотидов носит многофакторный характер и способствует регенерации периферических нервов. Нуклеотиды являются эссенциальными компонентами ДНК и РНК, которые влияют на метаболические пути и продуцируют энергию, играя важную роль в биосинтезе фосфолипидов и гликопептидов. Результаты ряда исследований in vitro свидетельствуют о том, что уридин и цитидин подвергаются инкорпорации на ранних стадиях нервного повреждения. В исследованиях на животных введение уридина трифосфата и цитидина монофосфата приводило к быстрому созреванию миелиновых оболочек и аксонов, а также увеличению скорости проведения по отдельным сенсорным и двигательным волокнам. Поскольку нервные клетки не могут синтезировать эти нуклеотиды, их необходимо вводить извне, особенно при хронической нейропатии (Müller D., 2002).
Эффективность применения нуклеотидов при терапии пацинтов НБ доказана в ряде исследований. Так, в ретроспективном исследовании (Lauretti G.R. et al., 2004) оценивали эффект применения комбинации цитидина, уридина с витамином B12 как вспомогательную терапию при терапии хронической нейропатической поясничной боли у пациентов с каудальным введением клонидина, лидокаина и дексаметазона. Всего в исследовании приняли участие 42 пациента: 21 направлен на проведение каудальной блокады (контрольная группа), 21 – получал комбинацию «цитидин + уридин + витамин B12» 2 раза в сутки в течение 28 дней. Результаты показали, что в контрольной группе была выше потребность в применении пероральных НПВП, чем в группе приема комбинации «цитидин + уридин + витамин B12», что свидетельствует об эффективности применения комбинации нуклеотидов с витамином B12 в терапии при НБ в спине.
В недавних исследованиях оценивалась эффективность и безопасность применения комбинации «уридин-5'-динатрия монофосфат + фолиевая кислота + витамин B12 (Нейристон®)» у 212 пациентов с НБ. Результаты продемонстрировали статистически значимое уменьшение общей оценки боли по опроснику боли (painDETECT Questionnaire — PDQ), интенсивность болевого синдрома, количество пораженных участков и степень болевого ощущения у пациентов, принимавших комбинацию нуклеотидов (Negrão L. et al., 2014; Negrão L., Nunes P., 2015).
На сегодняшний день имеется не много препаратов, которые бы действовали на уровне периферических нервов и способствовали бы их физиологической регенерации. Поэтому применение комплекса Нейристон®, в состав которого входит уридин-5'-динатрия монофосфат, витамин B12 и фолиевая кислота, обладающего регенераторным и обезболивающим эффектами, в комбинированной терапии может улучшить эффективность лечения при НБ.
Активные компоненты комплекса Нейристон® способствуют активизации собственных восстановительных процессов в поврежденных нервных тканях. Уридинмонофосфат, являющийся его основным компонентом, стимулирует синтез фосфолипидов, гликолипидов (сфинголипидов) и гликопротеинов — основных структурных компонентов клеточных мембран, что обеспечивает его регенеративное воздействие на нервные волокна. Фолиевая кислота и витамин B12 являются необходимыми коферментами для большинства метаболических реакций, за счет чего играют немаловажную роль в синтезе нуклеиновых кислот и белков. Комбинация активных веществ обеспечивает комплексное влияние на физиологические функции организма и приводит к ускорению восстановительных процессов в поврежденных нервных волокнах. Комплекс Нейристон® может быть рекомендован как источник питательных веществ, способствующих восстановлению поврежденных нервных волокон при таких состояниях как нейропатия, невралгия, люмбаго, поражение нервных структур метаболического характера, инфекционные нейропатии и т.д.
Таким образом, при лечении пациентов с НБ важен комплексный подход, включающий симптоматическую и патогенетическую терапию. Имеющиеся на сегодняшний день данные свидетельствуют, что применение прегабалина (Неогабин), а также комплекса нуклеотидов (Нейристон®), способствует эффективному купированию болевого синдрома, уменьшает выраженность тревожно-депрессивных расстройств, способствует активизации собственных восстановительных процессов в поврежденных нервных клетках, а также улучшению качества жизни пациентов с нейропатическим болевым синдромом.
Attal N., Cruccu G., Baron R. et al. (2010) European Federation of Neurological Societies: EFNS guidelines on the pharmacological treatment of neuropathic pain: 2010 revision. Eur. J. Neurol., 17: e1113–e1188.
Attal N., Cruccu G., Haanpaa M. et al. (2006) EFNS guidelines on pharmacological treatment of neuropathic pain. Eur. J. Neurol., 13: 1153–1169.
Baron R., Freynhagen R., Tölle T.R. et al. (2010) The Efficacy and Safety of Pregabalin in the Treatment of Neuropathic Pain Associated With Chronic Lumbosacral Radiculopathy. Pain, 150(3): 420–427. doi: 10.1016/j.pain.2010.04.013.
Finnerup N.B., Attal N. (2016) Pharmacotherapy of neuropathic pain: time to rewrite the rulebook? Pain Manag., 6(1): 1–3.
Finnerup N.B., Otto M., McQuay H.J. et al. (2005) Algorithm for neuropathic pain treatment — an evidence based proposal Pain, 118(3): 289–305.
Freeman R., Durso-Decruz E., Emir B. (2008) Efficacy, safety, and tolerability of pregabalin treatment for painful diabetic peripheral neuropathy: findings from seven randomized, controlled trials across a range of doses. Diabetes Care, 31(7): 1448–1454. doi: 10.2337/dc07-2105.
Lauretti G.C., Omals M., Pereira A.C. et al. (2004) Clinical evaluation of the analgesic effect of the cytidine-uridine-hydroxocobalamin complex as a coadjuvant in the treatment of chronic neuropathic low back pain. Column, 3(2): 73–76.
Martinez V., Attal N., Bouhassira D. et al. (2010) Chronic neuropathic pain: diagnosis, evaluation and treatment in outpatient services. Guidelines for clinical practice of the French Society for the Study and Treatment of Pain. Douleur analg., 23: 51–66.
Martinez V., Attal N., Vanzo B. et al. (2014) Adherence of French GPs to chronic neuropathic pain clinical guidelines: results of a cross-sectional, randomized, «e» casevignette survey. PLoS One, 9(4): e93855.
Moulin D.E., Clark A.J., Gilron I. et al. (2007) Pharmacological management of chronic neuropathic pain-consensus statement and guidelines from the Canadian Pain Society. Pain Res. Manag., 12(1): 13–21.
Müller D. (2002) Treatment of neuropathic pain syndromes. Results of an open study of the efficacy of a preparation based on pyrimidine nucleotides. Medien und Medizin Verlagsgesellschaft mbH&Co. KG, Munich.
Orita S., Yamashita M., Eguchi Y. et al. (2016) Pregabalin for Refractory Radicular Leg Pain due to Lumbar Spinal Stenosis: A Preliminary Prospective Study. Pain Res. Manag. (https://www.hindawi.com/journals/prm/2016/5079675/).
Negrão L., Almeida P., Alcino S. et al. (2014) Effect of the combination of uridine nucleotides, folic acid and vitamin B12 on the clinical expression of peripheral neuropathies. Pain Manag., 4(3): 191–196. doi: 10.2217/pmt.14.10.
Negrão L., Nunes P. (2015) Uridine monophosphate, folic acid and vitamin B12 in patients with symptomatic peripheral entrapment neuropathies. Pain Manag., 6(1): 25–29. doi: 10.2217/pmt.15.60.
Rosenstock J., Tuchman M., LaMoreaux L. et al. (2004) Pregabalin for the treatment of painful diabetic peripheral neuropathy: a double-blind, placebo-controlled trial. Pain, 110(3): 628–638.
Tolle T., Dukes E., Sadosky A. et al. (2006) Patient burden of trigeminal neuralgia: results from a cross-sectional survey of health state impairment and treatment patterns in six European countries. Pain Pract., 6(3): 153–160.
УКР. МЕД. ЧАСОПИС, 3 (137), Т. 1 – V/VI 2020 | www.umj.com.ua
к списку статей Найти врача